1. 배경지식
자폐증(자폐 스펙트럼 장애, Autism spectrum disorders)은 뇌 발달장애의 한 종류로서, 세계 인구의 약 2%가 앓고 있습니다. 사회성 및 인지능력 저하가 주요 증상으로 꼽히지만 정확한 메커니즘은 알려지지 않았습니다. 이전에 저희 연구실에서는 postsynaptic molecule 중 하나인 Shank2가 knockout 된 생쥐가 자폐증의 주요 증상들(사회성 저하, 반복행동 증가)을 가짐을 보인 바 있습니다. 또한, 이 증상에 excitatory 뉴런의 NMDA 수용체의 기능 저하가 관여되어 있으며, NMDA 수용체 agonist인 D-cycloserine(이하 DCS)를 처리해 주었을 때 생쥐의 행동과 NMDA 수용체의 기능이 모두 정상으로 돌아옴을 보였습니다. 이 결과들은 Shank2 knockout 생쥐가 자폐증 연구의 모델로 사용될 수 있는 가능성을 제시했지만, 시냅스 수준의 변화가 어떻게 행동의 변화로 연결되는지, neuron, circuit, region 수준에서의 mechanism을 제시하지는 못했습니다.
질문
사회성 감소에는 다양한 원인들을 생각할 수 있습니다. 제일 기본적으로는 감각이 망가져 아예 주변 사물들을 인지하지 못할 수 있습니다. 또는 일반적인 물체와 social target(e.g. 다른 생쥐)를 구분하지 못하거나, 사회적 교류 활동에서 보상을 느끼지 못할 수도 있습니다. 이런 후보들 중 Shank2 knockout 생쥐에서 보이는 사회성 저하의 mechanism을 알고 싶었고, 치료에 적용해볼 수 있을지를 알고 싶었습니다.
발견
Shank2 knockout 생쥐를 다양한 대상들(빈 chamber, 물체가 들어있는 chamber, social terget이 들어있는 chamber) 과 자유롭게 접촉하게 하며, 동시에 medial prefrontal cortex(이하 mPFC)에서 tetrode recording을 진행하였습니다. 각 뉴런 별로 복수의 대상들을 구분하는 firing pattern을 보임을 확인할 수 있었는데, 특히 Shank2 knockout 생쥐의 경우 각 뉴런이 반응하는 대상의 개수가 평균적으로 더 많음을 알 수 있었습니다. 비약적으로나마 예를 들자면, WT 생쥐 뉴런들의 경우 뉴런들이 일반적으로 1~2가지의 대상에만 특이적으로 반응하는 반면, Shank2 knockout 생쥐 뉴런들의 경우 3~4가지의 대상에 무분별하게 반응하는 것과 같이 생각해 볼 수 있습니다. 이로 인해 접촉대상별로 distinct한 circuit activity를 만들기 어렵고, mPFC에서 접촉대상에 대한 표상의 specificity가 떨어지는 것을 발견하였습니다.
기록된 뉴런들의 활동을 spike 형태에 따라 putative excitatory 뉴런과 putative inhibitory 뉴런으로 나눠 분석해보았을 때, Shank2 knockout 생쥐 putative inhibitory 뉴런들의 burst firing이 감소해 있는 것을 발견했습니다. 또한, gamma oscillation이 감소되어 있는 것을 확인하여, 이들과 관련되어 있는 Pv 뉴런에 집중하여 이후 실험들을 진행했습니다.
광유전학(optogenetics)적 자극을 통해 Pv 뉴런을 자극해주며 전기생리학(electrophysiology)적 실험들을 진행해, Shank2 knockout Pv 뉴런들이 주변 세포들을 충분히 inhibition 하지 못하고 있는 것을 발견했습니다. 이를 자세히 분석해보고자 이후 실험에서는 세포 하나에만 광유전학(optogenetics)적 자극을 줄 수 있는 pattern illuminator를 사용해 Pv 뉴런에 자극을 주며 전기생리학적 실험들을 진행했습니다. 그 결과 Pv 뉴런 사이의 전기적 시냅스를 통한 연결이 증가되어 있음을 확인했습니다. 전기적 시냅스는 간극연접(gap junction)을 통해 생성되는 뉴런 사이의 통로로, 보통 성체로 발달하는 과정에서 대부분 사라지지만, Pv 뉴런들 사이에서는 유지되어 dendrito-dendritic connection을 만드는 것으로 알려져 있습니다. Shank2 knockout 생쥐의 뇌에서는 자극을 받은 Pv 뉴런의 이웃 Pv 뉴런으로 전기적 시냅스를 통해 자극이 더 잘 전달되는 것을 확인하였습니다. 이는 이웃 Pv 뉴런들의 burst firing을 생성했으며, 이러한 효과는 전기적 시냅스를 block하는 mefloquine 처리에 의해 사라졌습니다.
또한 Shank2 knockout 생쥐의 Pv 뉴런에서도 NMDA 수용체의 기능이 저하되어 있는 것을 확인하였습니다. 이를 토대로 위와 같은 실험을 하며 DCS를 처리했을 때, 이웃 Pv 뉴런의 burst firing이 증가하는 것을 확인했습니다. 흥미롭게도 DCS를 처리를 통한 이웃 Pv 뉴런의 burst firing 증가 효과가 mefloquine 처리를 통해 사라진다는 점을 발견하였는데, 이는 NMDA 수용체가 전기적 시냅스와 협동하여 Pv 뉴런들의 burst firing을 만드는 것을 시사합니다.
종합해보면 Shank2 knockout 생쥐의 mPFC에서는, Pv 뉴런에서 감소해 있는 NMDA 수용체 기능으로 인해 Pv 뉴런들의 burst firing이 감소되어 있습니다. 또한, Pv 뉴런 사이의 전기적 시냅스가 WT에 비해 증가해 있습니다. 이에, 증가되어 있는 Pv 뉴런 사이의 전기적 시냅스 기능을 이용해 burst firing을 발생시켜 사회성을 다시 회복시켜 보고자 하였습니다. Shank2 knockout 생쥐의 mPFC에 있는 Pv 뉴런을 광유전학으로 자극하면서, 사회성을 알아볼 수 있는 three-chamber test를 진행한 결과, Shank2 knockout 생쥐의 사회성이 회복되는 것을 확인했습니다. 또한, 각 뉴런이 구분하는 대상의 수가 줄어든 것도 tetrode recording을 통해 확인함으로써, 행동학적인 회복뿐만 아니라, mPFC에서 접촉대상에 대한 표상도 회복됨을 발견했습니다.
후속
자폐증과 연관된 것으로 알려진 유전자는 1,000가지가 넘습니다. (SFARI gene) 이들 중 많은 수가 생쥐 모델로 제작되어 연구되고 있으며, 저희 연구실에서도 수십 종류의 자폐 모델 생쥐들을 활용해 연구를 진행 중입니다. 이번에 밝힌 자폐증의 사회성 저하 모델이 다양한 자폐 모델 생쥐에 적용되는지 확인하여 일반화시켜보는 것은, 자폐증을 이해하고 치료하는 데 있어 중요한 연구가 될 것 같습니다. 또한, 자폐증 분야에서 전기적 시냅스의 역할이 최초로 조명된 만큼, Pv neuron network에서 전기적 시냅스의 기능을 알아보는 것도 좋은 연구가 될 것 같습니다.
소감
좋은 기회로 이 연구에 참여하게 되고, 마무리 할 수 있게 되어서 너무 기쁩니다. 긴 과정이었지만, 실험 결과와 내용이 재미있어 지치지 않고 계속할 수 있었던 것 같습니다. 제가 겪었던 과정에 많은 분들의 도움이 있었음을 잊지 않고, 저도 좋은 연구자 및 조력자가 될 수 있도록 계속 노력하겠습니다.
기타
늘 많은 가르침 주시는 김은준 교수님과 사수님이신 이은이 박사님께 진심으로 감사드립니다. 각자 맡은바 고생이 많으셨던 공동 저자분들, 그리고 긴 과정 동안 많은 도움 주신 연구실 선후배분들께도 감사의 말을 전합니다.
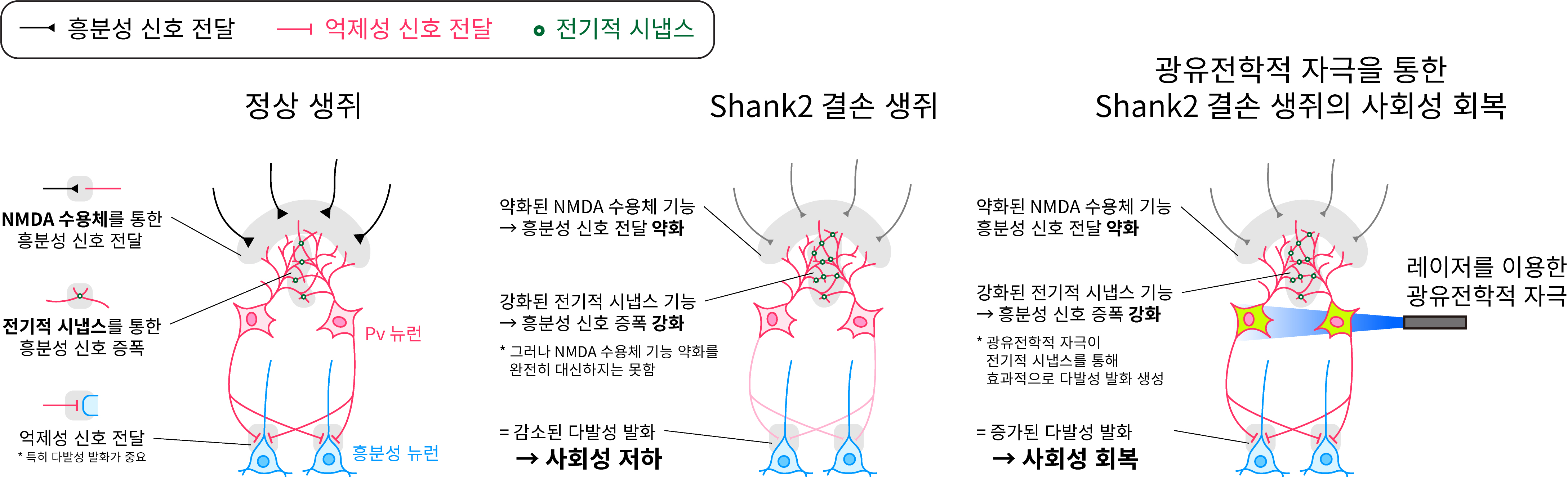
Shank 2 결손 생쥐의 사회성 저하 및 광유전학 자극을 통한 회복 모식도







 조혜림 (크로마틴 생물학 연구실, 이대엽 교수님)
조혜림 (크로마틴 생물학 연구실, 이대엽 교수님)
 김재현(감각처리 연구실, 이승희 교수님)
김재현(감각처리 연구실, 이승희 교수님)



















