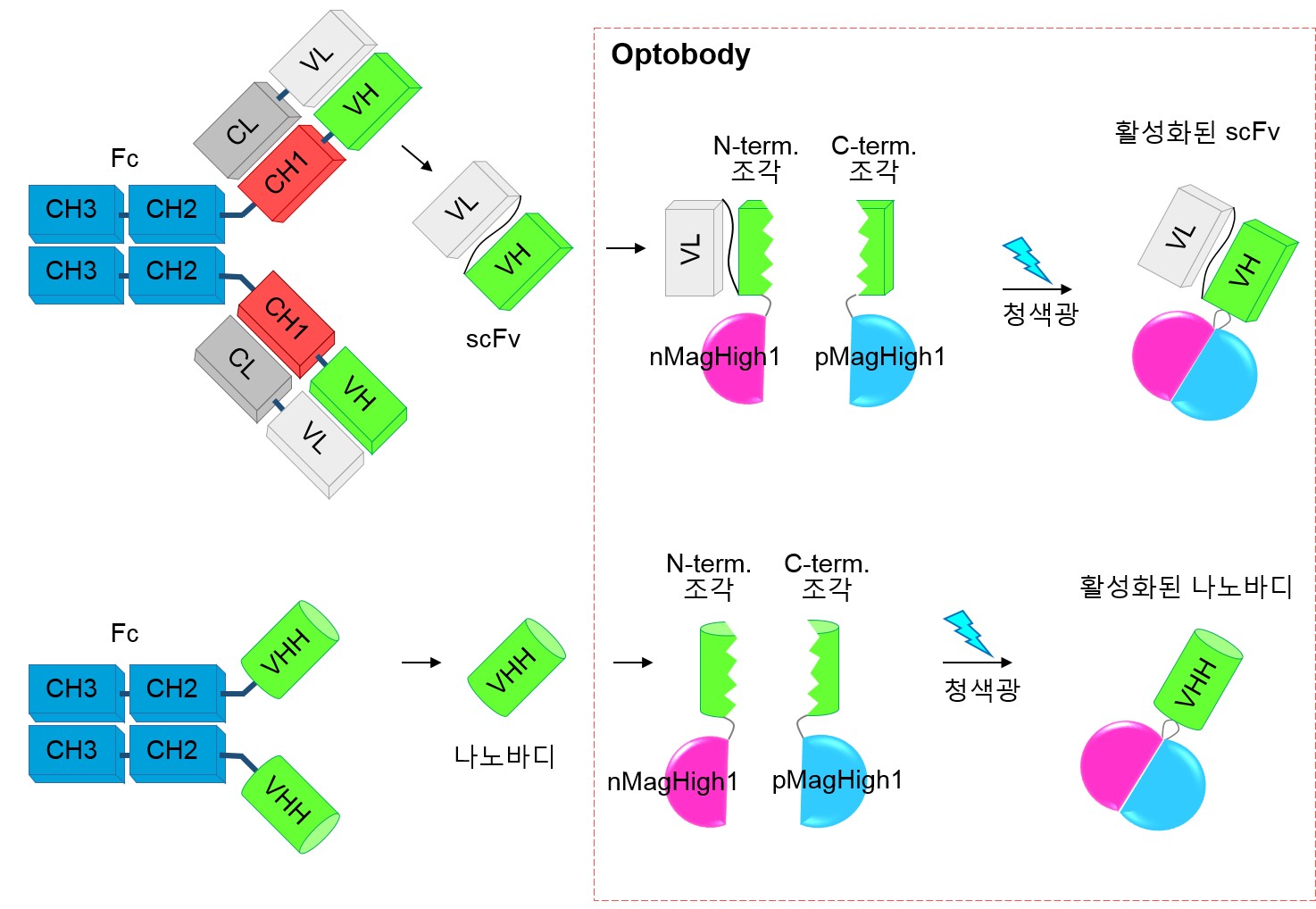
<그림 1> 항체조각과 Optobody 모식도
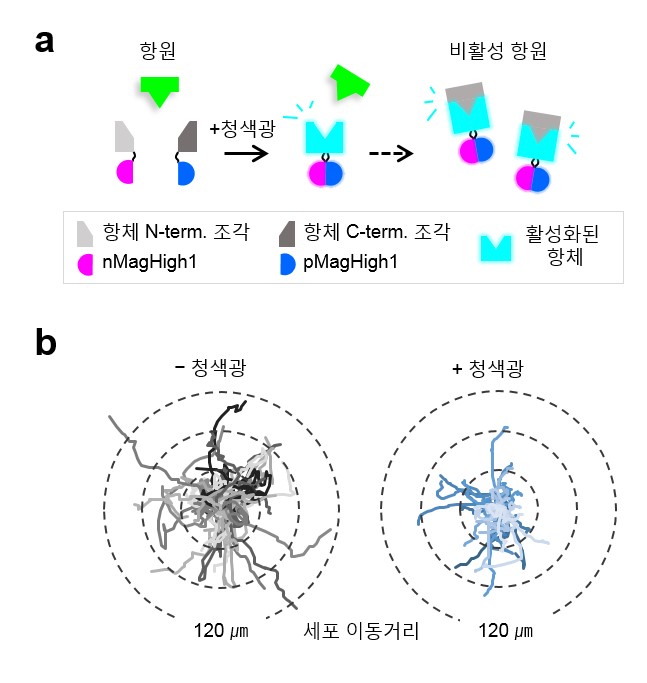
<그림 2> 광활성화된 항체에 의한 항원의 비활성 및 기능 억제
1. 배경지식
항체는 면역반응의 핵심 물질이며 질병 치료제로도 사용 중에 있습니다. 항체를 직접적인 질병 치료제로 사용하는 경우 항체 단백질을 정제하여 투여해주는데, 이때 투여하는 순간부터 항체가 작동하기 시작해 원하는 부위가 아닌 다른 부위에서 작동하는 경우가 있습니다. 또한 항체를 이용한 면역반응 치료에 있어서도 원하는 부위와 시간대에 항체를 활성화시킬 수 없어 부작용을 초래합니다. 의약적 측면 뿐만 아니라 생명과학 및 공학 연구에서 항체의 활성을 조절하는 기술은 극히 제한적이며, 현재 사용되고 있는 기술은 항체 발현을 유도하는 것이 전부입니다. 하지만 항체의 발현을 유도하는 기술은 그 반응 효과가 느리고, 특정 세포 혹은 세포 내 특이적으로 조절하기 어려우며 비가역적이라는 한계점을 가집니다.
2. 질문:
1) 항체의 활성을 빛으로 조절하는 항체광유전학 기술 개발이 가능한가
2) 개발한 항체광유전학 기술이 범용적으로 여러 항체에 적용 가능한가
3)항체광유전학 기술이 내생단백질의 기능 억제제로 사용 가능한
3. 발견:
본 연구에서 개발한 항체광유전학 기술은 항체 구조물 중 가장 작은 단위인 VH 도메인을 둘로 쪼개 비활성화 시키고 이를 빛으로 재결합시켜 활성화하는 기술 (Optogenetically activated intracellular antibody; Optobody)입니다. 항체가 항원과 직접 결합하는 부위인 상보성결정부(CDR)들을 분리시킴으로써 항체를 비활성화 시키고, 청색광에 반응해 결합하는 단백질을 이용해 쪼개진 항체를 재결합시켜 활성을 유도하였습니다. 본 기술의 범용성을 넓히기 위해 항체 조각 (Antibody fragment) 중 나노바디와 scFv 에 본 기술을 접목시켰고, 모두 성공적으로 청색광에 의한 활성을 유도하였습니다. 이를 통해 다양한 내생단백질을 빛 특이적으로 인지 및 결합하는 항체를 구현할 수 있었습니다. 더 나아가 내생단백질 억제제로 사용 중인 항체 조각 기술을 이용해 내생단백질의 기능을 빛에 의해 시공간적으로 저해시키는 것에 성공하였습니다.이는 광활성 항체를 이용해 내생단백질의 기능을 억제시키는 새로운 개념의 기술을 보여준 것이고, 질병 치료제로서의 가능성 또한 제시하였습니다.
4. 후속
본 연구는 항체의 활성을 직접적으로 조절하며, 특히 빛을 이용해서 시공간적으로 항체 활성을 일으킬 수 있다는 점에서 획기적입니다. 항체 및 항체 조각들이 다양한 생명과학 및 공학 분야에서 사용되고 있기 때문에 optobody 기술이 폭넓게 응용될 수 있다고 기대합니다. 또한 기존에 치료 의약품으로 이용되고 있는 항체 혹은 항체를 매개체로 이용 중인 세포 치료제 등에 적용될 수 있으므로 새로운 개념의 항체 의약품으로 발전 될 가능성이 있기 때문에 이와 관련된 연구를 진행하고자 합니다.
5. 소감
본 연구를 진행하면서 제일 어려웠던 점은 다양한 항원을 인지하는 항체를 얻는 것이었습니다. 특히 내생단백질 억제제로 사용 중인 항체는 그 단백질 서열이 공개되지 않아 임의로 제작 및 사용이 어려웠습니다. 따라서 다양한 국내외 연구진에게 항체를 요청하여 얻게 되었고, 그분들이 흔쾌히 항체를 공유해주어 본 기술의 범용성을 증명할 수 있었습니다. 연구는 혼자만의 프로젝트로 진행하는 것이 아닌 인류를 위해 함께 진행하는 것임을 배울 수 있었고, 앞으로도 이런 마음가짐을 가지고 연구활동을 하고자 합니다.
6. 기타
본 연구의 아이디어를 제시해주시고 좋은 결과로 마무리 할 수 있도록 지도해주신 허원도 교수님께 감사드립니다. 또한 공동연구 제안을 흔쾌히 받아주시고 짧은 리비전 기간에 훌륭한 결과를 얻게 도와주신 오병하 교수님과 이한솔 박사님께 감사드립니다. 더불어 서로를 응원하며 함께 성장해가는 연구실 동료들 모두 감사합니다. 끝으로 오랜 시간 저의 공부를 지지해주시고 응원해주신 부모님과 가족들, 상욱오빠, 사랑스러운 규빈이에게 감사 인사를 전하며, 앞으로도 계속 성장하는 모습 보여드리도록 노력하겠습니다. 감사합니다.







 서예지 (바이오이미징&광유전학 연구실, 허원도 교수님)
서예지 (바이오이미징&광유전학 연구실, 허원도 교수님)
 김기정 (에피제네틱스 구조생물학 연구실, 송지준 교수님)
김기정 (에피제네틱스 구조생물학 연구실, 송지준 교수님)



















